NORMA OFICIAL MEXICANA NOM-095-SSA1-1994, QUE ESTABLECE LAS ESPECIFICACIONES SANITARIAS DEL DISPOSITIVO INTRAUTERINO "T" DE COBRE MODELO 380A.
Al margen un sello con el Escudo Nacional, que dice: Estados Unidos Mexicanos.- Secretaría de Salud.
FRANCISCO J. HIGUERA RAMIREZ, Director General de Control de Insumos para la Salud, por acuerdo del Comité Consultivo Nacional de Normalización de Regulación y Fomento Sanitario, con fundamento en los artículos 39 de la Ley Orgánica de la Administración Pública Federal; 13 A fracción I, 194 fracción II, 194 Bis, 195, 196, 197, 201, 210, 262 fracción V y demás aplicables de la Ley General de Salud; 3 fracción XI, 38 fracción II, 40 fracción XIII, 41, 43 y 47 de la Ley Federal sobre Metrología y Normalización; 2 fracción III inciso v), 12, 14, 67, 1147 fracción VII y demás aplicables del Reglamento de la Ley General de Salud en Materia de Control Sanitario de Actividades, Establecimientos, Productos y Servicios; 8 fracción IV y 12 fracción II del Reglamento Interior de la Secretaría de Salud, y
NORMA OFICIAL MEXICANA NOM-095-SSA1-1994, QUE ESTABLECE LAS ESPECIFICACIONES SANITARIAS DEL DISPOSITIVO INTRAUTERINO "T" DE COBRE MODELO 380A.
INDICE
0. PREFACIO
1. OBJETIVO Y CAMPO DE APLICACION
2. REFERENCIAS
3. DEFINICIONES
4. SIMBOLOS Y ABREVIATURAS
5. ESPECIFICACIONES
6. METODOS DE PRUEBA
7. EMPAQUE Y ETIQUETADO
8. MUESTREO
9. CONCORDANCIA CON NORMAS INTERNACIONALES
10. BIBLIOGRAFIA
11. OBSERVANCIA DE LA NORMA
12. VIGENCIA
PREFACIO
Este documento describe al Dispositivo Intrauterino "T" de Cobre, Modelo 380A, los accesorios para su inserción dentro de la cavidad uterina, las especificaciones técnicas de los materiales, e incluye las pruebas de control de calidad y los métodos de prueba que deben realizarse al producto.
Deben realizarse una amplia variedad de pruebas e inspecciones a las materias primas y a los componentes utilizados para la producción del Dispositivo Intrauterino "T" de Cobre Modelo 380A. Estas pruebas de control de calidad deben llevarse a cabo en diferentes intervalos a través de todas las etapas de fabricación, que van desde la recepción de las materias primas hasta la liberación del lote del producto terminado estéril, listo para su empleo.
Las pruebas de control están diseñadas para asegurar, controlar y verificar lote a lote la calidad del producto y su efectividad hasta por diez años.
Las Unidades Administrativas que participaron en la elaboración de esta norma son: Dirección General de Control de Insumos para la Salud; las Instituciones: Instituto Mexicano del Seguro Social (Jefatura de Control de Calidad), Dirección General de Normas de la Secretaría de Comercio y Fomento Industrial, la Cámara Nacional de la Industria Farmacéutica (CANIFARMA): Sección de Productos Auxiliares para la Salud y la Cámara Nacional de la Industria de la Transformación (CANACINTRA): Consejo Paramédico y los establecimientos: Implementos Plásticos, S.A., Insumos para la Salud, S.A. de C.V. y Laboratorios Alpha, S.A. de C.V.
1. Objetivo y campo de aplicación.
1.1 Objetivo.
Esta Norma establece las especificaciones y las características de calidad que debe cumplir el Dispositivo Intrauterino "T" de Cobre Modelo 380A (DIU TCu 380A), señalando los métodos de prueba, sus límites y tolerancias, así como señalar las propiedades físicas, químicas y mecánicas del dispositivo intrauterino (DIU), de los accesorios para su inserción dentro de la cavidad uterina, del empaque, del etiquetado, de la esterilización y de su almacenamiento, para que empleado de acuerdo a la Norma Oficial Mexicana NOM-005-SSA2-1993, De los Servicios de Planificación Familiar, se obtengan los resultados ahí enunciados.
1.2 Campo de Aplicación.
Esta Norma es de observancia obligatoria para todos los Dispositivos Intrauterinos "T" de Cobre Modelo 380A, de fabricación nacional o extranjera, en todo el territorio nacional.
2. Referencias.
| NOM-Z-12 | Muestreo para la Inspección de Atributos (Parte 1, 2 y 3). |
| NOM-005-SSA 2-1993 | De los Servicios de Planificación Familiar. |
| NOM-008-SCFI | Sistema General de Unidades de Medida. |
| ISO-7857 | International Standard Intrauterine Devices Part 1 - Part 2 - Part 3. |
| ISO-7439 | Mechanical Contraceptives - Intrauterine Devices. |
3. Definiciones.
3.1 Descripción del DIU TCu modelo 380A:
El DIU TCu modelo 380A es un dispositivo activo, de material plástico en forma de "T", el cual tiene ensambladas piezas de cobre de una pureza del 99.99%, producto de uso médico, estéril, fabricado con materiales grado médico y de pureza conocida, que empleado adecuadamente cumple la función de ser un anticonceptivo de carácter temporal, de alta efectividad y seguridad hasta por diez años de su uso continuo.
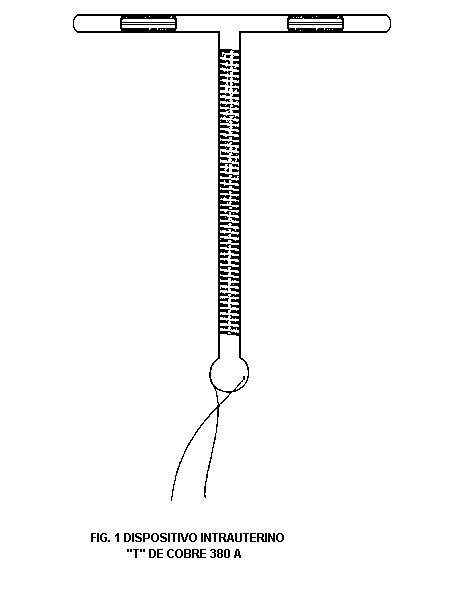
Está constituido por siete piezas que incluyen: al DIU como tal y a los accesorios que se utilizan para su inserción dentro de la cavidad uterina (Figuras 1 y 2).
Los componentes del producto son:
Del DIU:
- Cuerpo de plástico moldeado en forma de "T".
- Monofilamento largo o monofilamento corto.
- Dos anillos de cobre.
- Alambre de cobre.
De los accesorios para la inserción:
- Tubo insertor.
- Tope.
- Embolo insertor.
3.1.1 Materiales Inactivos del DIU.
3.1.1.1 Para la fabricación del cuerpo de la "T", los materiales deben ser una mezcla al 77% de plástico grado médico y 23% de sulfato de bario "FEUM", que asegure su radio-opacidad y sus propiedades fisicoquímicas. Las dimensiones aproximadas son de 36 mm en la rama vertical y de 32 mm en la rama horizontal. El propósito del DIU en forma de "T" es adaptarse a la anatomía de cavidad uterina y el de soportar el alambre y los anillos de cobre que al liberar el metal a las secreciones endometriales, éste disminuye en forma importante la capacidad de fecundación y transporte o movimiento de los espermatozoides.
3.1.1.2 El monofilamento debe ser fabricado con un material plástico grado médico y fácilmente visible. El monofilamento se anuda firmemente a la esfera de la rama vertical del cuerpo de la "T". El propósito del monofilamento es ayudar en la localización del DIU in situ, así como en su remoción.
3.1.2 Materiales Activos.
3.1.2.1 Alambre de cobre OFE-101 (libre de oxígeno), enrollado en la rama vertical, duro, redondo, con una pureza del 99.99%, con el restante 0.01% de otros elementos, habiendo sido examinados, cuantificados y comparados contra los resultados de análisis espectrográficos específicos.
3.1.2.2 Dos anillos de cobre OFE-101 (libre de oxígeno), colocados en los brazos de la rama horizontal, duro, redondo, con una pureza del 99.99%, con el restante 0.01% de otros elementos, habiendo sido examinados, cuantificados y comparados contra los resultados de análisis espectrográficos específicos.
El cobre debe tener un área total de 380 ± 23 mm2.
3.2 Accesorios para la inserción.
3.2.1 Tubo insertor de plástico grado médico, semirrígido, que se utiliza para colocar el DIU TCu 380A en la cavidad uterina a través del endocérvix.
3.2.2 Tope fabricado de plástico semirrígido de diferente color al tubo insertor para que contraste. Tiene un orificio al centro por medio del cual se ensambla con el tubo insertor. El diámetro del orificio debe facilitar el deslizamiento justo del tope sobre el tubo insertor, y además permitir su retención a la distancia deseada del endocérvix. Se utiliza para señalar en el tubo insertor la profundidad de la cavidad uterina, previamente determinada (por histerometría), para lo cual el tubo es introducido a través del canal cervical en la cavidad uterina.
3.2.3 Embolo insertor fabricado con plástico semirrígido, de diferente color al tubo insertor para que contraste. Se utiliza para liberar el DIU TCu 380A del tubo de inserción hacia la cavidad uterina.
4. Símbolos y abreviaturas.
| ºC | Grado Celsius |
| cm3 | Centímetro cúbico |
| DIU | Dispositivo Intrauterino |
| DIU TCu Modelo 380A | Dispositivo Intrauterino "T" de Cobre Modelo 380A |
| g | Gramo |
| k | Grado Kelvin |
| mg | Miligramo |
| min | Minuto |
| 1M | Solución Molar |
| MGA | Métodos Generales de Análisis de la FEUM |
| MGA 0561 | Metales Pesados. |
| MGA 0089 | Análisis Térmico |
| MGA 0351 | Espectrofotométrico de Absorción Infrarroja |
| MGA 0381 | Esterilidad |
| mm | Milímetro |
| mm2 | Milímetro cuadrado |
| FEUM | Farmacopea de los Estados Unidos Mexicanos |
| USP | Farmacopea de los Estados Unidos Americanos |
| Vel. de iny. cm3/s | Velocidad de inyección centímetros cúbicos por segundo |
| N | Newton |
| 1N | Solución Normal |
| ppm | Partes por millón |
| % | Por ciento |
| s | Segundo |
| SSA | Secretaría de Salud |
5. Especificaciones.
5.1 Plástico grado médico para el cuerpo del DIU en forma de "T", el monofilamento, el tubo insertor, el tope y el émbolo insertor.
| PRUEBA | LIMITES |
| Infrarrojo | El espectro infrarrojo de la muestra debe ser idéntico al patrón de referencia. |
| Extractables | Debe pasar la prueba de extractables para plásticos Clase II. |
| Inyección sistémica | Debe pasar la prueba. |
| Intracutánea | Debe pasar la prueba. |
| Implantación | Debe pasar la prueba. |
| Metales pesados | No mayor a 1 ppm. |
| Oxido de etileno residual máximo | 5 ppm. |
| Esterilidad | Debe ser estéril. |
5.2 Sulfato de bario grado FEUM para proporcionar radio-opacidad y ciertas propiedades fisicoquímicas al cuerpo del DIU en forma de "T".
| PRUEBA | LIMITES |
| Identidad | Debe pasar la prueba. |
5.3 Mezcla de plástico grado médico y sulfato de bario grado FEUM para el cuerpo del DIU en forma de "T".
| PRUEBA | LIMITES |
| Residuo de la ignición | 20 - 24% de contenido de sulfato de bario (promedio de 2 muestras o de 4 si fuera necesario). |
5.4 Bióxido de titanio grado FEUM para el cuerpo del DIU en forma de "T" y el émbolo insertor.
| PRUEBA | LIMITES |
| Identidad | Debe pasar la prueba. |
5.5 Plástico grado médico coloreado para el monofilamento.
| PRUEBA | LIMITES |
| Residuo de la ignición | No más del 1% en contenido de bióxido de titanio u otro colorante (promedio de 2 muestras o de 4 si fuera necesario). |
5.6 "T" de plástico moldeada (Fig. 3).
| PRUEBA | LIMITES |
| Dimensiones (mm) | |
| Brazo horizontal: Longitud |
31.6 a 32.3 |
|
diámetro |
1.5 a 1.7 |
| Rama vertical: Longitud |
35.7 a 36.2 |
| diámetro |
1.5 a 1.7 |
| Diámetro del orificio superior |
0.3 a 0.5 |
| Diámetro de la esfera |
2.9 a 3.1 |
| Diámetro del orificio de la esfera |
0.3 a 0.6 |
| Flexibilidad (mm) |
5.2 a 6.3 |
| Memoria | El valor promedio de recuperación debe ser máximo de 5.0 mm. |
| Inyección sistémica | Debe pasar la prueba. |
| Intracutánea | Debe pasar la prueba. |
| Implantación | Debe pasar la prueba. |
| Metales pesados | No mayor de 1 ppm. |
| Radio-opacidad | El material básico del DIU debe ser opaco a los rayos X. |
5.7 Monofilamento largo o corto del DIU.
| PRUEBA |
LIMITES |
||
| Dimensiones (mm) | Largo | Corto | |
| Longitud | 290 a 310 | 105 a 125 | |
| diámetro | 0.20 a 0.30 | 0.20 a 0.30 | |
| Fuerza de rompimiento (N) | Debe resistir como mínimo 8.8 | ||
| Inyección sistémica | Debe pasar la prueba | ||
| Intracutánea | Debe pasar la prueba | ||
| Implantación | Debe pasar la prueba | ||
| Metales pesados | No mayor de 1 ppm | ||
5.8 Anillos de cobre colocados en el brazo horizontal del DIU.
| PRUEBA |
LIMITES |
|||
| Análisis espectrográfico | Contenido mínimo de cobre 99.99% | |||
| Contenido máximo de otros elementos: | ||||
| Pb | 2 ppm | Te | 3 ppm | |
| Cd | 1 | Sb | 2 | |
| Fe | 10 | As | 3 | |
| Ni | 5 | P | 1 | |
| Hg | 1 | Ag | 50 | |
| Sn | 1 | Bi | 1 | |
| Zn | 2 | Mn | 2 | |
| Se | 5 | |||
| Dimensiones (mm) | ||||
| Diámetro externo | 2.1 a 2.2 | |||
| diámetro interno | 1.6 a 1.7 | |||
| longitud | 4.9 a 5.2 | |||
| Peso (mg) | 61.3 a 78.7 | |||
| Resistencia al anclaje (N) | 6.8 a 16.7 | |||
5.9 Alambre de cobre colocado en la rama vertical del DIU.
| PRUEBA |
LIMITES |
|||
| Análisis espectrográfico | Contenido mínimo de cobre 99.99%. | |||
| Contenido máximo de otros elementos | ||||
| Pb | 2 ppm | Te | 3 ppm | |
| Cd | 1 | Sb | 2 | |
| Fe | 10 | As | 3 | |
| Ni | 5 | P | 1 | |
| Hg | 1 | Ag | 50 | |
| Sn | 1 | Bi | 1 | |
| Zn | 2 | Mn | 2 | |
| Se | 5 | |||
| Dimensiones (mm) | ||||
| Longitud | 390 a 410 | |||
| Diámetro | 0.25 a 0.26 | |||
| Peso (mg) | 165 a 187 (100 cm de alambre de cobre pesar entre 436 a 472 mg). | |||
5.10 Tubo insertor.
| PRUEBA |
LIMITES |
|
| Dimensiones (mm) | ||
| Longitud | 194 a 208 | |
| Diámetro externo | 4.3 a 4.5 | |
| Diámetro interno | 3.6 a 3.8 | |
| Inyección sistémica | Debe pasar la prueba | |
| Intracutánea | Debe pasar la prueba | |
| Implantación | Debe pasar la prueba | |
| Metales pesados | No mayor de 1 ppm | |
5.11 Tope.
| PRUEBA |
LIMITES |
| Dimensiones (mm) | |
| Diámetro del orificio | 4.2 a 4.4 |
| Fuerza de desplazamiento (N) | 3.5 a 6.2 |
5.12 Embolo.
| PRUEBA |
LIMITES |
| Dimensiones (mm) | |
| Longitud del sujetador a la punta | 188 a 193 |
| Diámetro de la punta | 2.5 a 3.0 |
5.13 "T" de Cobre Modelo 380A, con filamento corto y largo.
| PRUEBA | LIMITES |
| Dimensiones (mm) | |
| Diámetro externo de los | 2.1 a 2.3 |
| anillos de cobre | |
| ensamblados | |
| Distancia entre el extremo | 5.0 a 5.8 |
| del anillo de cobre y la | |
| punta del brazo horizontal | |
| de la "T". | |
| Peso (mg) | |
| Alambre de cobre | 165 a 187 |
| Punto de amarre (mm) | |
| Distancia entre la esfera y el | No mayor a 2.5 |
| nudo del monofilamento | |
| Radio-opacidad | Debe ser opaco a los rayos X |
| Area total de cobre (mm2) | 357 a 403 |
| Acabado | Debe estar libre de fisuras, deformaciones, burbujas, oquedades, rebabas, rugosidades, roturas, material extraño, nódulos, piezas faltantes, marcas de esmerilado y poros. Todas las piezas de los componentes deben ser lisas y de color uniforme. |
| Apariencia del Cobre | El cobre en condiciones normales expuesto al aire se cubre lentamente de una pátina de carbonato básico que se adhiere al metal y lo protege de toda ulterior corrosión. El cambio de color de la superficie del cobre no disminuye su eficacia anticonceptiva. |
6. Métodos de prueba.
Los disolventes y reactivos utilizados deben ser grado reactivo, a menos que se indique otro grado.
El agua empleada debe ser destilada a no ser que se indique otra pureza.
El material de vidrio utilizado debe ser de borosilicato de bajo coeficiente de expansión térmica, lavado previamente con mezcla crómica y de ser necesario con ácido nítrico caliente, enjuagado con suficiente agua estéril para inyección. Secar, esterilizar y si se utiliza óxido de etileno para esterilizar, desgasificar durante 48 horas.
Los aparatos empleados deben estar debidamente calibrados.
6.1 Infrarrojo.
6.2 Pruebas biológicas in-vivo.
6.2.1 Fundamento.
Estas pruebas se basan en determinar la respuesta biológica en animales de laboratorio, ante la presencia de porciones de plásticos o de sus respectivos extractos.
6.2.2 Condiciones de las pruebas.
Efectuar cada prueba en no menos de 8 unidades provenientes de un mismo lote, de distintas estibas y empaques colectivos.
6.2.3 Reactivos y materiales.
La preparación de las muestras, soluciones y estándares estériles y apirogénicos debe efectuarse en una campana de flujo laminar confinada en un área aséptica.
Todo el material de vidrio, así como los reactivos y medios para la extracción de la muestra deben ser estériles y libres de pirógenos.
- Mezcla crómica.
- Acido nítrico.
- Cloruro de metileno.
- Alcohol etílico.
- Acetona.
- Cloruro de sodio.
6.2.4 Aparatos y equipos.
- Baño de agua con control de temperatura y termómetro.
- Autoclave capaz de mantener una temperatura de 394 K ± 2 K (121ºC ± 2ºC) equipada con termómetro y calibrador de presión.
- Horno, de preferencia un modelo de circulación forzada, con una temperatura de operación en el intervalo de 323 K a 343 K (50ºC a 70ºC).
- Recipientes para extracción. Utilizar recipientes como: Ampulas o tubos de ensayo para cultivo, de vidrio Tipo I, con tapón de rosca, con un forro elastomérico adecuado, el cual debe estar completamente protegido con un disco sólido inerte de 50 a 75 mm de espesor y que puede fabricarse con una resina de politetrafluoroetileno.
- Tijeras de acero inoxidable para cortar la muestra, lavadas con detergente, enjuagadas perfectamente con agua destilada, con acetona y cloruro de metileno, antes de utilizarlas.
- Agujas hipodérmicas, calibre 15 G, con 19 mm de longitud.
- Mandril o estilete.
- Agujas calibre 26 G, con 24 mm de longitud.
- Jeringas.
- Rasuradora.
- Control negativo de plástico FEUM
6.2.5 Preparación y condiciones de los medios para la extracción de las muestras.
Solución de cloruro de sodio 0.9%: Pesar 9 g de cloruro de sodio, disolver en agua y llevar a un volumen final de 1000 cm3, esterilizar en autoclave a 394 K (121ºC) durante 20 minutos.
Agua
Polietilenglicol 400.
Solución de alcohol 1 en 20 en cloruro de sodio para inyección: Diluir 1 cm3 de alcohol para cada 20 cm3 de solución de cloruro de sodio al 0.9%.
Aceite vegetal: utilizar aceite de sésamo refinado recientemente o aceite de semilla de algodón.
El aceite de sésamo o de semilla de algodón que se utiliza en las pruebas debe cumplir con la siguiente especificación: A tres conejos preparados como se indica en el inciso 6.2.1 Animales de prueba, inyectar intracutáneamente 0.2 cm3 de aceite en diez sitios por animal y observar el sitio de inyección, a las 24, 48 y 72 horas siguientes a la inyección. Ningún sitio debe presentar edema y eritema, mayor de 5 mm de diámetro.
6.2.6 Preparación de la muestra.
Tanto para las pruebas de inyección sistémica como para la prueba intracutánea puede usarse el mismo extracto, si se desea. Seleccionar y subdividir las piezas de plástico a analizar, en fragmentos de aproximadamente 5 x 0.3 cm, hasta el equivalente a 60 cm2 de superficie total. Remover el material particulado de las muestras fraccionadas y del control negativo, como sigue: Colocar la muestra en una probeta de vidrio tipo I, con tapón y graduada a 100 cm3, añadir cerca de 70 cm3 de agua inyectable. Agitar aproximadamente 30 s y descartar el agua, repetir este paso, y secar las piezas preparadas para extraer con aceite vegetal en un horno a temperatura que no exceda de 323 K (50ºC) (Nota.- No limpiar la muestra ni con lienzo seco ni húmedo, ni enjuague con agua ni con solventes orgánicos, etc.).
6.2.7 Preparación del blanco.
Colocar individualmente en un recipiente de extracción 20 cm3 de cada medio de extracción y tratarlos de la misma forma que los de la muestra.
6.2.8 Preparación de los extractos.
Colocar una muestra de plástico preparada adecuadamente en un recipiente de extracción, añadir 20 cm3 del medio de extracción, apropiado de acuerdo a la Tabla I. Repetir estas instrucciones para cada medio de extracción que requiera la prueba. Preparar también un blanco con 20 cm3 de cada medio de extracción para inyectar en paralelo y comparar. Extraer en autoclave a 394 K (121ºC) durante 60 minutos, en horno a 343 K (70ºC) por 24 horas o a 323 K (50ºC) durante 72 horas. Dejar el tiempo necesario para que el líquido dentro del recipiente alcance la temperatura de extracción.
TABLA 1
MEDIOS DE EXTRACCION UTILIZADOS PARA CADA CLASE DE PLASTICO
|
CLASE DE PLASTICO |
MEDIO DE EXTRACCION | ||
|
I |
V |
VI |
|
|
X |
X |
X |
Cloruro de sodio para inyección. |
|
X |
X |
X |
Solución de alcohol 1 en 20 en cloruro de sodio para inyección. |
|
X |
X |
Polietilenglicol 400 | |
|
X |
X |
Aceite vegetal | |
Las condiciones de extracción no deben en ninguna instancia producir cambios físicos tales como fusión o licuefacción de las piezas de plástico, ya que estos cambios provocan una disminución del área superficial. Puede tolerarse una ligera adherencia entre las piezas.
Si se utilizan tubos de cultivo para extracciones con aceite vegetal en autoclave, sellar los tapones de rosca con una cinta testigo para esterilizar.
Dejar enfriar los recipientes hasta cerca de la temperatura ambiente pero no menos de 293 K (20ºC), agitar vigorosamente durante varios minutos y decantar inmediatamente cada extracto, en forma aséptica dentro de un recipiente estéril y seco. Almacenar los extractos a una temperatura entre 293 K y 303 K (20ºC y 30ºC), y no usarlos hasta después de 24 horas. Es muy importante el contacto del medio de extracción con la superficie de las piezas de plástico, así como el tiempo y la temperatura durante la extracción, el enfriamiento, la agitación, el proceso de decantación, el manejo aséptico y almacenaje de los extractos después de la extracción.
6.2.9 Inyección sistémica.
Esta prueba se utiliza para evaluar la respuesta sistémica a los extractos de materiales de prueba después de inyectarse en ratones.
Animales de prueba: utilizar ratones blancos, sanos que no hayan sido utilizados previamente, con un peso entre 17 y 23 g, de una misma cepa y ofrecer a satisfacción agua y alimento de composición conocida para animales de laboratorio.
Procedimiento: Seleccionar 40 ratones y separarlos en 8 grupos de 5 ratones cada uno. Pesar y marcar cada uno de los animales de cada grupo de prueba. Agitar cada extracto vigorosamente antes de separar cada dosis de inyección para asegurar la completa distribución del material extraído. Inyectar cada uno de los animales con los extractos de muestras y blanco por la vía de administración y dosis que corresponda al peso del animal de acuerdo a la tabla siguiente, excepto el extracto obtenido con polietilenglicol 400 y su blanco correspondiente que deben diluirse con 4.1 volúmenes de cloruro de sodio, para obtener una solución con una concentración de aproximadamente 200 mg de polietilenglicol por cm3.
TABLA 2
DOSIS Y VIA DE ADMINISTRACION DEL BLANCO, MUESTRA PROBLEMA Y MEDIOS DE EXTRACCION UTILIZADOS
|
No. de Grupo |
Extract:E Blanco:B |
Medio de Extracción |
Dosis por Kg |
Vía de Adminis. |
Vel. de Iny. cm3/s |
|
1 2 |
E B |
Cloruro de sodio para inyección |
50 cm3 |
I.V. |
0.1 |
|
3 4 |
E B |
Sol. alcohol 1 en 20 en cloruro de sodio para inyec. |
50 cm3 |
I.V. |
0.1 |
|
5 6 |
E B |
Polietilenglicol 400 |
10 g |
I.P. |
--- |
|
7 8 |
E B |
Aceite vegetal (sésamo o de semilla de algodón) |
50 cm3 |
I.P. |
--- |
I.V. Vía de Administración: Intravenosa en vena caudal.
I.P. Vía de Administración: Intraperitoneal.
Observar los animales inmediatamente después de la inyección y a las 4, 24, 48 y 72 horas posteriores.
Interpretación.
Si durante el periodo de observación ninguno de los animales tratados con los extractos de la muestra presenta una reacción significativamente mayor que los animales tratados con el blanco, la muestra con las especificaciones de la prueba.
Si alguno de los animales tratados con la muestra presenta ligeros síntomas de toxicidad y no más de uno de los animales muestra síntomas severos de toxicidad o muere, repita la prueba utilizando grupos de 10 ratones cada uno. En la prueba de repetición las especificaciones de la prueba se cumplen si ninguno de los animales tratados con la muestra presenta una reacción significativamente mayor que la observada en los animales tratados con el blanco.
6.2.10 Intracutánea.
Esta prueba se utiliza para evaluar una respuesta local a los extractos de los plásticos a probar, después de inyectar intracutáneamente a los conejos.
Animales de prueba: Seleccionar conejos blancos, sanos que no hayan sido utilizados en ninguna prueba, de piel delgada, que puedan rasurarse con facilidad y que estén libres de irritación o trauma mecánico.
Preparación de la muestra: Proceder de acuerdo a lo establecido anteriormente utilizando polietilenglicol 400 como medio de extracción.
Preparación de blanco: Proceder de acuerdo a lo establecido anteriormente utilizando polietilenglicol 400 como medio de extracción.
Procedimiento.
El día de la prueba, rasurar completamente la piel del lomo del animal hacia ambos lados de la columna vertebral, sobre un área de prueba suficientemente larga. Evitar la irritación o el trauma mecánico. Retirar el pelo suelto por medio de vacío. Si es necesario limpiar la piel suavemente con el alcohol diluido y secarla antes de inyectar.
Antes de llenar la jeringa con la dosis de inyección, agitar cada extracto vigorosamente para asegurar la distribución completa de la materia extraída.
Diluir cada gramo del extracto de la muestra preparada con polietilenglicol 400 y su blanco correspondiente con 7.4 volúmenes de cloruro de sodio inyectable, para obtener una solución que contenga una concentración de aproximadamente 120 mg de polietilenglicol por cm3.
Inyectar intracutáneamente 0.2 cm3 de cada extracto de muestra en 10 sitios sobre uno de los lados de cada uno de los conejos. En forma semejante inyectar 0.2 cm3 del blanco correspondiente en 5 sitios del otro lado de cada conejo.
Examinar los sitios de inyección a las 24, 48 y 72 horas después de la inyección para detectar evidencia de reacción tisular como eritema, edema y escaras. Para facilitar el examen tratar la piel suavemente con alcohol diluido y rasurar la piel si es necesario.
Valorar las observaciones sobre una escala numérica para el extracto de la muestra y el blanco respectivamente, de acuerdo a la Tabla 3.
TABLA 3
EVALUACION DE LAS REACCIONES EN PIEL
| Eritema y formación de escaras | Valor |
| eritema ausente | 0 |
| eritema ligero (escasamente perceptible) | 1 |
| eritema bien definido | 2 |
| eritema de moderado a severo | 3 |
| eritema severo (enrojecimiento intenso) a formación ligera de escaras (daño intenso) | 4 |
| Formación de edema | Valor |
| edema ausente | 0 |
| edema muy ligero (escasamente perceptible) | 1 |
| edema ligero (bordes del área bien definidos por inflamación) | 2 |
| edema moderado (inflamación aproximada de 1 mm) | 3 |
| Edema severo (inflamación mayor a 1 mm que se extiende más allá del área de exposición) | 4 |
Interpretación.
La muestra cumple con las especificaciones de la prueba si el promedio de reacciones de la muestra no es significativamente mayor que el promedio de reacción del blanco.
Si el resultado es dudoso, repetir la prueba en tres conejos más con extractos preparados recientemente.
Las especificaciones de la prueba se cumplen si en la prueba de repetición el promedio de reacción para el extracto de la muestra no es significativamente mayor que el promedio de reacción para el blanco.
6.2.11 Implantación.
Todos los componentes que conforman el DIU, incluyendo el monofilamento y el tubo insertor deben someterse a la prueba de implantación y demostrar ser inertes o no irritantes, histológicamente.
Animales de prueba.
Seleccionar conejos adultos, sanos, con peso no menor a 2.5 kg y cuyos músculos paravertebrales sean lo suficientemente grandes para permitir el implante de las tiras de prueba.
Preparación de la muestra.
Cortar la muestra en 8 tiras de 10 x 1 mm y 4 tiras del control negativo de plástico FEUM del mismo tamaño.
Los bordes de las tiras deben ser tan suaves comos sea posible para evitar un trauma mecánico adicional al implante.
Insertar cada tira limpia dentro de una aguja e introducir a un tubo de cultivo con tapón de rosca, esterilizar por un procedimiento adecuado.
Procedimiento.
Realizar la prueba en un área limpia.
El día de la prueba o 20 horas antes, rasurar la piel del lomo de los animales, hacia ambos lados de la columna vertebral.
Retirar el pelo suelto por medio de vacío.
Anestesiar los animales con un agente anestésico de uso común a un grado de profundidad suficiente para prevenir rompimientos musculares como la contracción.
A una distancia de 2.5 a 5 cm de la línea media de la espina dorsal, implantar 4 tiras de la muestra en el músculo paravertebral sobre un lado de la columna de cada de dos conejos, separadas una de la otra aproximadamente 2.5 cm.
De manera similar implantar dos tiras de control negativo de plástico FEUM en el músculo paravertebral opuesto de cada animal.
Insertar un estilete estéril dentro de la aguja para mantener la tira de plástico en el tejido cuando se retire la aguja. Si se observa un sangrado excesivo después de la implantación de una tira, colocar un duplicado en otro sitio. El cierre de la incisión es completo después de la implantación.
Mantener los animales por un periodo no menor de 72 horas. Sacrificar los animales al final de este periodo, administrando una sobredosis de un agente anestésico.
Dejar transcurrir el tiempo suficiente para que el tejido al cortar no sangre. Examinar macroscópicamente el área de tejido circundante a la porción central de cada tira implantada, utilizar una lente de aumento si es necesario.
El tejido inmediato alrededor de las tiras del control negativo de plástico FEUM en muestra normal y completamente libre de hemorragia, película o encapsulación.
Interpretación.
Las especificaciones de la prueba se cumplen si en cada conejo la reacción a no más de una en cuatro muestras es significativamente mayor que la reacción de las tiras del control negativo de plástico FEUM
6.3 Metales pesados: Seguir el método FEUM. MGA 0561.
6.4 Identidad: Seguir los métodos generales de análisis de la FEUM: MGA 0089 Análisis Térmico, MGA 0351 Espectrofotografía de Absorción Infrarroja.
6.5 Residuo de la ignición: Seguir el método general de análisis MGA 0751 de la FEUM.
6.6 Dimensiones: Utilizar una regla metálica para medir longitudes y un Vernier o cualquier otro instrumento adecuado para medir diámetros.
6.7 Flexibilidad:
6.7.1 Esta prueba consiste en medir la deflexión de mm cuando se somete el brazo horizontal de la "T" a un peso de 20 g colocado a 1.2 cm del cruce de la "T" durante 30 s.
6.7.2 Equipo: Utilizar una pesa calibrada de 20 g y dos pinzas.
6.7.3 Procedimiento: Las unidades utilizadas para esta prueba deberán tener por lo menos 24 h de haber sido moldeadas y después de mantenerlas a una temperatura de 295.5 K a 298.5 K (22.5ºC a 25.5ºC). Las lecturas hechas a diferentes temperaturas pero dentro de los límites de 293 K a 302 K (20ºC a 29ºC), pueden corregirse restando 0.125 unidades por cada grado de temperatura que sobrepase los 297 K (24°C) y sumando la misma cantidad por cada grado de temperatura por debajo de los 297 K (24ºC), sin embargo cualquiera que sea la temperatura seleccionada, ésta deberá ser constante por lo menos durante 6 h. y no variar en ± 274.5 K (± 1.5ºC).
6.8 Memoria: Se mide en términos de recuperación después de una flexión aguda. El brazo horizontal se dobla y se inserta dentro del orificio del tubo insertor a una profundidad de 6 mm. En esa posición deben permanecer durante 5 min, y medirse después de 1 min de haber liberado el brazo horizontal de la "T", colocando la "T" sobre una plantilla en forma de los ejes X, Y, graduados.
6.9 Radio-opacidad: Exposición a los rayos X.
6.9.1 Este método de prueba está enfocado a determinar si el artículo tiene el grado de radiopacidad especificado para su aplicación como un dispositivo en el cuerpo humano y nos da la posibilidad de localizarlo dentro del cuerpo.
6.9.2 El aparato de rayos X utilizado es de tipo médico.
6.9.3 El espécimen se coloca sobre el chasis del aparato de rayos X y sobre éste una placa de aluminio con 99% de pureza y 10, 15 o 30 mm de espesor.
6.9.4 Cuando la radiografía revelada es examinada a través de la luz, la imagen del espécimen debe ser claramente visible como un área de luz brillante en contraste con un fondo obscuro.
6.10 Fuerza de rompimiento: Seguir el método descrito en ISO 7857/1. Intrauterine devices - Part: Determination of breaking force.
6.10.1 Esta prueba consiste en medir la tensión necesaria para romper el monofilamento.
6.10.2 El aparato para medir la tensión debe ser capaz de reproducir las mediciones en forma constante y cumplir con los siguientes requisitos:
6.10.2.1 Fuerza límite de 0 a 100 N.
6.10.2.2 Velocidad de separación de 3.3 ± 0.3 mm/s (200 ± 20 mm/min).
6.10.2.3 Registro automático de la tensión aplicada durante la prueba (utilizar papel registrador).
6.10.3 Procedimiento: La prueba debe realizarse con monofilamentos estériles. Separar el monofilamento del DIU y colocar un extremo en la pinza superior del aparato y el otro extremo en la pinza inferior, aplicar una tensión hasta que el monofilamento se rompa. Si la ruptura ocurre en cualquiera de las dos pinzas, seleccionar otras muestras y repetir la prueba. Medir la fuerza de rompimiento en Newtons.
6.11 Análisis espectrográfico: Esta prueba debe realizarse tanto para los anillos de cobre como para el alambre de cobre. Se cuantifica por medio de un espectrofotómetro de absorción atómica.
6.12 Peso: Se utiliza una balanza analítica con exactitud de 0.1 mg.
6.13 Fuerza de desplazamiento.
Seleccionar al azar una muestra representativa de topes y colocarlos cada uno en un tubo insertor, dejarlos permanecer ahí de 24 a 96 horas, la resistencia al desplazamiento cuando se aplica una fuerza debe estar entre 360 g y 630 g. Cuando esta prueba se realiza con 300 unidades, no más de 7 piezas pueden presentar una resistencia por arriba de 900 g o 7 piezas por debajo de 180 g.
6.14 Area total de cobre: Calcular la superficie de los dos anillos y del alambre de cobre, utilizando la siguiente fórmula:
a = 2 Pi*r*l
Donde:
a = área total del cobre
Pi = 3.1416
r = radio
l = longitud
6.15 Esterilización: Se utiliza el óxido de etileno como gas esterilizante. Los resultados deben ser de acuerdo al Método General de Análisis MGA 0381 Esterilidad de la Farmacopea de los Estados Unidos Mexicanos.
6.16 Contenido residual de óxido de etileno.
Fundamento.
Se basa en la determinación cuantitativa a través de la espectrofotometría del óxido de etileno residual contenido en el producto en su empaque final y que ha sido esterilizado con este gas.
Descripción del aparato de extracción.
El aparato está constituido con un matraz balón de fondo redondo de unos 140 mm de diámetro y 1000 cm3 de capacidad, dotado de tres bocas (a, b y c) con juntas esmeriladas destinadas a colocar en la boca (b) un refrigerante (B) de 330 mm de longitud, colocándole arriba en la entrada de aire un tubo capilar, el cual va conectado a un frasco lavador (1) de 200 3 de capacidad (ver figura 4 Aparato de Extracción).
El matraz descansa sobre un calentador redondo (2) y en la boca (a) un refrigerante (A) que debe estar orientado a dos frascos (3 y 4) de Deware montados en serie, de 220 mm de altura y 25 mm de diámetro, los cuales deben contener hielo picado y en cuyo interior se encuentran dos frascos (3a y 4a); la boca (c) es para la adición de soluciones. Finalmente un tubo en ángulo unido al frasco (4a) y a un frasco lavador (5) de 200 cm3 de capacidad (ver figura 4 Aparato de Extracción).
Estabilización del aparato de extracción: Introducir en el frasco lavador (1) una solución preparada por disolución de 1.7 g de clorhidrato de hidroxilamina en 3.3 cm3 de trietanolamina y 100 cm3 de agua (ver figura 4 Aparato de Extracción).
Colocar dentro del matraz balón (2) de 100 a 150 cm3 de agua, dentro de los dispositivos (3a y 4a) 40 cm3 de agua a 273 K (0ºC) y dentro del frasco lavador (5) 50 cm3 de agua (ver figura 4 Aparato de Extracción).
Poner a ebullición el contenido del matraz balón hasta observar en la trampa de agua (5) la salida de burbujas a una velocidad de 4 burbujas por segundo (ver figura 4 Aparato de Extracción).
Equipo y reactivos:
Espectrofotómetro de absorción visible equipado con:
Lámpara de tungsteno.
Celdas de absorción de vidrio o cuarzo.
Matraz de vidrio de fondo redondo dotado de tres bocas.
Tres juntas esmeriladas.
Dos refrigerantes.
Dos frascos lavadores.
Dos frascos Deware con un frasco cada uno en su interior.
Tubería de vidrio.
Balanza analítica con exactitud de 0.0001 g.
Material usual de laboratorio.
Sal sódica del ácido cromotrópico.
Clorhidrato de hidroxilamina.
Trietanolamina.
Etilen glicol.
Solución de hidróxido de sodio 0.5 N.
Solución de peryodato de sodio 0.1 M.
Solución de sulfito de sodio al 11%.
Acido sulfúrico.
Solución de ácido sulfúrico 0.5 N.
Solución de ácido sulfúrico 18 N.
Preparación de las soluciones patrón.
Pesar con exactitud 1.4 g de etilen glicol diluir a 1000 cm3 con agua, tomar una alícuota de 10 cm3 de esta solución y diluir 100 cm3 con agua.
Colocar en una serie de cinco matraces volumétricos de 100 cm3 alícuotas de 1, 2, 3, 4 y 5 cm3, respectivamente, de la solución anterior de etilen glicol. Agregar a cada uno de ellos, 2 cm3 de solución de peryodato de sodio 0.1 M dejándolo en contacto permanente durante un tiempo de 15 min, con agitación permanente. Adicionar una alícuota de 2 cm3 de solución de sulfito de sodio al 11% y aforar a 100 cm3 con agua.
Transferir una alícuota de 5 cm3 de la solución proveniente del primero de los matraces tratados anteriormente, a un matraz volumétrico de 10 cm3, colocar en el hielo, adicionar gota a gota 5 cm3 de una mezcla que contenga 0.10 g de la sal sódica del ácido cromotrópico en 2 cm3 de agua y 50 cm3 de ácido sulfúrico.
Repetir la misma operación con los cuatro matraces restantes.
Colocar los tubos de ensayo a baño María durante 10 min, enfriar a temperatura ambiente y completar a 10 cm3 con ácido sulfúrico 18 N.
Estas soluciones contienen, respectivamente, el equivalente a 0.5, 1.0, 1.5, 2.0 y 2.5 ppm como óxido de etileno.
Preparación de la muestra. Seleccionar al azar 10 muestras estériles de un mismo lote de esterilización.
Pesar con exactitud cerca de 16 g de las "T" permitiendo que todas sus partes incluyendo el hilo, se recorten en fragmentos de aproximadamente 0.10 g y colocarlos dentro del matraz balón descrito anteriormente.
Destilar de 45 a 50 min. Transcurrido el tiempo de destilación indicado, desmontar los frascos 3a y 4a y vaciar su contenido dentro de un matraz con tapón esmerilado de 150 cm3 de capacidad, lavar los frascos vaciando las aguas del lavado en el matraz*. Adicionar 1 cm3 de ácido sulfúrico de 0.5 N, cerrar herméticamente el matraz y colocarlo en un baño María en ebullición durante 1 h. Dejar enfriar a temperatura ambiente, neutralizar la solución con 1 cm3 de hidróxido de sodio 0.5 N y trasvasar a un matraz volumétrico de 100 cm3. Lavar el matraz de 150 cm3, vaciar las aguas del lavado al matraz volumétrico* y aforar con agua. Transferir una alícuota de 5 cm3 de la solución anterior a un matraz volumétrico de 100 cm3 y continuar el tratamiento de la muestra de igual manera que la solución patrón desde la oxidación peryódica.
Preparación del blanco: Colocar en un matraz con tapón esmerilado de 150 cm3 de capacidad, 80 cm3 de agua, adicionar 1 cm3 de ácido sulfúrico 0.5 N, cerrar herméticamente el matraz y colocarlo en un baño María en ebullición durante 1 h. Dejar enfriar a temperatura ambiente, neutralizar la solución con 1 cm3 de hidróxido de sodio 0.5 N y trasvasar a un matraz volumétrico de 100 cm3, lavar el matraz de 150 cm3, vaciar las aguas del lavado al matraz volumétrico* (*cuidar que la cantidad de agua utilizada para lavar los frascos 3a y 4a, así como los matraces de 150 cm3 con tapón esmerilado, mencionados anteriormente, no sobrepase el total de 100 cm3, incluyendo la muestra) y aforar con agua. Transferir una alícuota de 5 cm3 de la solución anterior a un matraz volumétrico de 100 cm3 y continuar el tratamiento del blanco de igual manera que las soluciones patrón desde la oxidación peryódica.
Procedimiento: Obtener la absorbancia de las soluciones patrón de referencia, de menor a mayor concentración, a una longitud de onda de máxima absorbancia de aproximadamente 570 nm y ajustar el aparato con el blanco. Posteriormente medir la absorbancia de la preparación de la muestra problema en las mismas condiciones.
Cálculos: Graficar las lecturas de las absorbancias obtenidas con las soluciones del patrón de referencia, contra sus concentraciones respectivas en óxido de etileno y trazar la curva sabiendo que 1.409 g de etilen glicol corresponden a 1.0 g de óxido de etileno. Para determinar la concentración de óxido de etileno en la muestra, interpolar en la curva patrón la absorbancia obtenida y multiplicar por el factor de dilución obtenido.
Interpretación de resultados: El resultado obtenido no deberá ser mayor de 5 ppm y deberá estar dentro de los límites establecidos.
7. Empaque y etiquetado.
7.1 Empaque primario.
Deberá contener un DIU TCu modelo 380A con sus accesorios para su inserción y un instructivo impreso con la información requerida y aprobada por la SSA. El producto en su empaque primario debe ser estéril.
Descripción
Empaque transparente al menos en una de sus caras, de dimensiones adecuadas para contener al producto. Su diseño debe asegurar:
7.1.1 Adecuada protección del contenido durante el manejo, transporte y almacenamiento.
7.1.2 Mantener la esterilidad del contenido bajo condiciones secas, limpias y almacenamiento con ventilación adecuada.
7.1.3 Riesgo mínimo de contaminación para el producto al sacarlo del empaque primario para su aplicación.
7.1.4 El empaque primario, una vez abierto, no puede ser resellado sin que se note que ha sido previamente abierto.
7.2 Empaque secundario.
Una cantidad conveniente de empaques primarios (por ejemplo 25, 50, 100, etc.) deben ser empacados en una o más cajas, las cuales deben ser lo suficientemente rígidas para proteger el contenido durante su manejo y almacenamiento.
7.3 Etiquetado.
Las leyendas del producto tanto en su empaque primario, secundario y embalaje, deben estar escritas en idioma español, en caracteres legibles e indelebles. Deben cumplir con las disposiciones de la Secretaría de Salud, del Art. 210 de la Ley General de Salud.
7.4 Instructivo de uso.
El producto debe contener un instructivo para la inserción del DIU TCu Modelo 380A en la cavidad uterina, que especifique claramente cada paso del procedimiento ilustrado con programas que correspondan al escrito, además de la siguiente información:
7.4.1 Advertencias.
7.4.2 Preparación preliminar.
7.4.3 Precauciones.
7.4.4 Contraindicaciones.
8. Muestreo.
Se recomienda el uso de la Norma Oficial Mexicana NOM-Z-12 Vigente.
9. Concordancia con normas internacionales.
Esta Norma concuerda parcialmente con las siguientes publicaciones:
- ISO/TR 7439-1981 (E). Mechanical contraceptives Intra-uterine Devices.
- ISO 7857/1 Intrauterine Devices, Part 2 Determination of Breaking Force.
- ISO 7857/3-1983 (E). Intrauterine Devices, Part 3 Packaging and Labelling.
- FDA Registration: NDA-18-680. Copper T model 380A.
- A Manual for Testing Finished Devices Produced Under Licence from The Population Council.
- Manufacture Specifications on the Copper T Model TCu 380A and TCu 200B brand of Intra-uterine Copper Contraceptives. The Population Council.
10. Bibliografía.
- Ley General de Salud.
- Farmacopea de los Estados Unidos Mexicanos (FEUM) Vigente.
- United States Pharmacopea (USP) XXII NF XVII, 1990.
- Sivin Irving. Greenslade Forrest, Schmidt Frederick and Waldman, Sandra N. (1992). "The Copper T 380 Intrauterine Device" The Population Council".
- Tatum Howard J., Connell-Tatum Elizabeth B. Waldman Sandra N., and Greenslade Forrest C. (1989). "The New Para Gard Copper T 380A Intrauterine Device" Medical Digest Vol. 9 No. 1 pp. 1.
- WHO (1987) "Mechanism of action, safety and efficacy of intrauterine devices" WHO Technical Report Series 753.
- The Population Council (1991) "Copper T Intrauterine Device" The Population Council Up Date No. 2 January.
- Out Look (1993). "DIUs: Seguros y Eficaces para Muchas Mujeres".
- Out Look PATH Vol. 10 No. 2 pp. 1.
- Out Look (1992) "Diversidad de métodos anticonceptivos: Importancia de asegurar a las clientes una variedad de opciones" Out Look PATH Vol. 10 No. 1 pp 1.
- Population Report (1988). "Los DIUs: Un nuevo examen" Dispositivos Intrauterinos Serie B No. 5 pp 1.
- Química Teórica y Descriptiva. Sienko-plane, Aguilar 1972, México, pp 517.
- IMMS, Métodos Generales de Análisis. Determinación por Radiografía de la Radiopacidad.
11. Observancia de la Norma.
La vigilancia del cumplimiento de la presente Norma corresponde a la Secretaría de Salud, cuyo personal realizará la verificación y la vigilancia que sean necesarias.
12. Vigencia.
La presente Norma entrará en vigor con su carácter de obligatorio, a partir del día siguiente de su publicación en el Diario Oficial de la Federación.
México, D.F., a 1 de febrero de 1996.- El Director General de Control de Insumos para la Salud, Francisco J. Higuera Ramírez.- Rúbrica.




Fecha de publicación: 28 de mayo de 1996